El titular del Juzgado de Instrucción número 1 de Málaga ha acordado continuar el caso del «falso omeprazol» administrado a bebés, que en realidad recibieron minoxidil (crecepelo), contra cuatro personas, dos directivos y dos empleados de la empresa malagueña que etiquetó el producto.
Por otra parte, el magistrado Antonio Navas Hidalgo ha decretado el archivo provisional de la investigación a los laboratorios que lo fabricaron en La India, a la compañía que lo importó a España y a las farmacias que lo comercializaron en varias provincias.
Así lo dictamina en un auto dictado en el marco de las diligencias practicadas por estos hechos, que podrían constituir delitos contra la salud pública y de lesiones por imprudencia o negligencia profesional grave.
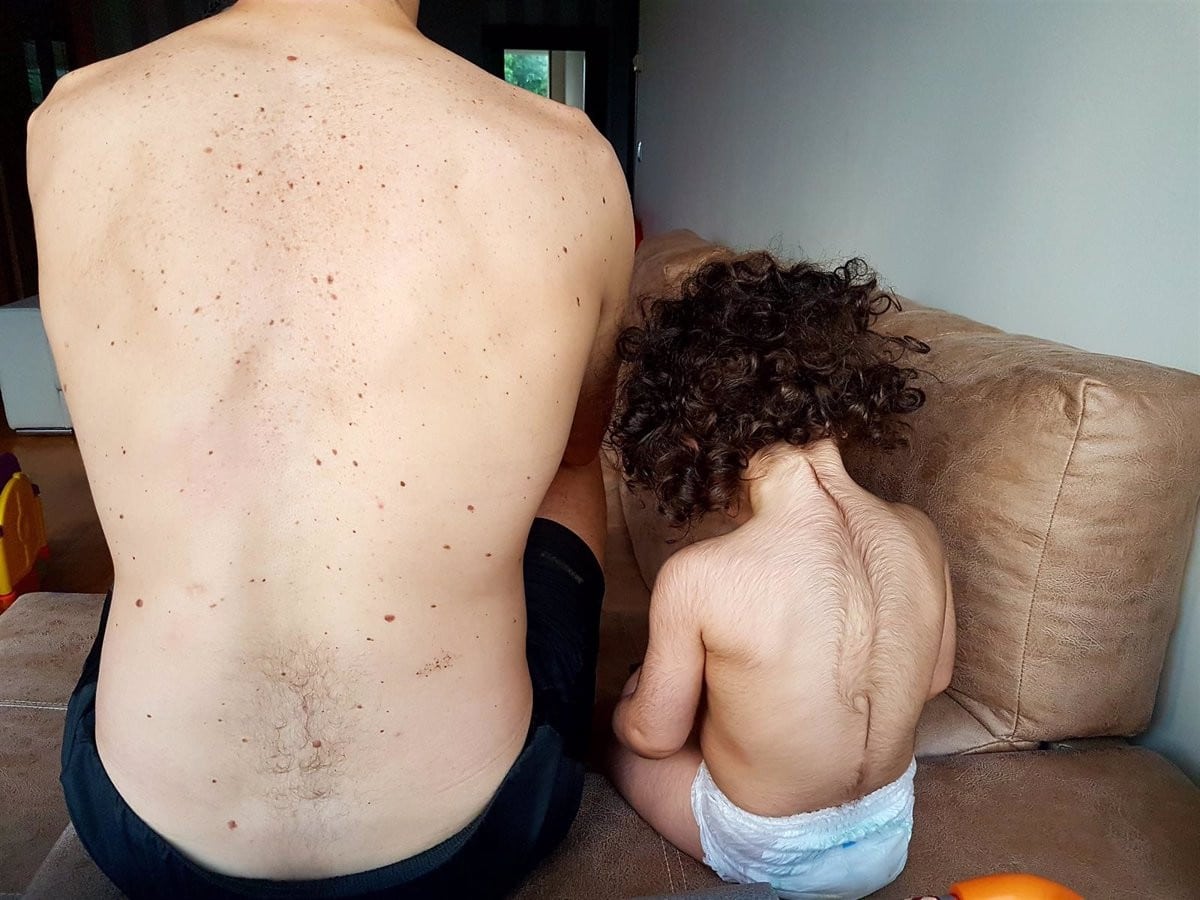
El falso omeprazol se administró por error a una veintena de bebés de varias provincias que sufren hipertricosis, enfermedad que provoca el crecimiento de vello por todo el cuerpo. Las autoridades sanitarias confirmaron en septiembre de 2019 que había 23 menores afectados, con edades comprendidas entre los dos meses y los siete años: diez en Cantabria, diez en Andalucía y tres en la Comunidad Valenciana.
El instructor imputa lo ocurrido a Farmaquímica Sur S.L., la firma andaluza que etiquetó el medicamento: una fórmula magistral como si fuera protector de estómago, pero «adulterado» con crecepelo, y que recibieron niños de Torrelavega y de otras localidades de Granada, Castellón o Bilbao, que han sufrido «importantes daños corporales y secuelas».
En concreto, están investigados el representante legal y administrador único de la empresa y el director técnico de la misma, así como dos trabajadores relacionados con la actividad profesional negligente investigada, por su presunta participación en la misma.
El magistrado sostiene en su resolución que las diligencias practicadas hasta ahora por estos hechos evidencian que «existen indicios y motivos razonables y suficientes» para atribuir su perpetración a los directivos y empleados de la empresa.
Para llegar a esta conclusión, ha tenido en cuenta las distintas pruebas practicadas, como declaraciones, documental aportada, el informe policial de la investigación y de la Agencia Española de Medioambiente y Productos Sanitarios (AEMPS).
La AEMPS detectó en una inspección a las instalaciones de la empresa «numerosas irregularidades» relacionadas con el control de las operaciones de fraccionamiento y reenvasado.
También constató que durante el fraccionamiento del «omeprazol» se hizo igualmente de ‘minoxidil’, por lo que «resulta factible admitir que aquel pudo contaminarse con éste en el procedimiento de fraccionamiento del lote original», indica el juez.
Por contra, considera que la empresa fabricante y la importadora no serían responsables de la «adulteración» del producto, en la que tampoco participaron las farmacias que lo vendieron a sus clientes, según expone.
DE LA INDIA A ESPAÑA
El instructor explica que un lote de un producto o medicamento, supuestamente omeprazol y fabricado por unos laboratorios de La India, llegó con su pertinente certificado de análisis al aeropuerto de Niza (Francia) en abril de 2018. Desde allí fue introducido y distribuido en España por una empresa y adquirido a continuación -en mayo- por Farmaquímica, donde fue fraccionado en lotes para su posterior distribución en el mercado.
Pero antes de eso, la empresa malagueña efectuó el correspondiente análisis técnico del producto a granel que determinó que el principio activo que contenía el envase original adquirido era ‘omeprazol’. Al año siguiente, en julio de 2019, tras una alerta de calidad se realizaron análisis en los laboratorios de la Agencia Española de Medicamentos y Productos Sanitarios que determinaron que el lote en cuestión contenía en realidad minoxidil.
Se acordó la retirada del producto del mercado y una inspección a la entidad, a las áreas y actividades relacionadas con la recepción, almacenamiento, fraccionamiento (reenvasado) y control de calidad (servicio subcontratado).
Por un lado, se comprobó que el principio activo en el envase original procedente de los laboratorios de La India era omeprazol y, por otro, la existencia de diferentes «prácticas contrarias a los principios de las normas de correcta fabricación», relativas a la falta de trazabilidad y controles de las operaciones de fraccionamiento y reenvasado por parte de Farmaquímica.
Las pesquisas policiales verificaron que en 2018 y 2019 se habían realizado «numerosas fragmentaciones» de lotes originarios con principio activo omeprazol y también con minoxidil.
Posteriormente, se detectaron dos lotes más que contenían igualmente crecepelo y que a principios de 2019 vendió Farmaquímica a farmacias de Cantabria, Bilbao, Granada y Castellón.
Estas oficinas distribuyeron a su vez el producto entre los consumidores y como resultado se ocasionaron «importantes lesiones y secuelas» a los menores afectados, según los informes forenses.
Este procedimiento se abrió a raíz de que la Fiscalía de Málaga acordara remitir al juzgado las diligencias de investigación abiertas de oficio. En paralelo, en 2019 se interpuso una denuncia ante el Juzgado de Instrucción número 4 de Torrelavega (Cantabria), que se inhibió en favor del de Málaga.